



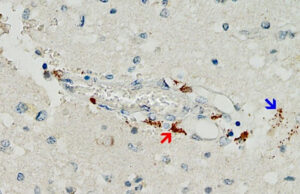
Vaktsiini ogavalgu ladestumine aju otsmikusagaras. Foto: Michael Mörz / MDPI (SARS-CoV-2 ogavalgu tuvastamine ajukoes vaktsiini poolt indutseeritud entsefaliidiga surnud patsiendilt immunohistokeemia abil. Pruuni pigmendi ladestumine näitab ogavalgu olemasolu väikese veresoone seinas (punane nool) ja ümbritseva ajukoe mitmes gliiarakus (sinine nool).)
Alloleva, üsna murrangulise dokumendi on koostanud teadlased ja arstid Michael Palmer ja Sucharit Bhakdi vastusena advokaadile, kes vaidlustab COVID-19 vaktsiinide heakskiite ja volitusi oma koduriigis.
Organisatsiooni Doctors for COVID Ethics veebilehel avaldatud artiklis vastavad meditsiinidoktorid üle 30 teadsuuringule ja allikale viidates kolmele küsimusele:
Kokkuvõtteks leiavad dr Palmer ja dr Bhakdi, et pärast mRNA vaktsiinide kasutamist COVID-19 vastu on arvukalt teateid kesknärvisüsteemi häiretest. Nende häirete hulka kuuluvad insult, ajuverejooks ja entsefaliit. Ei ole vajalik, et aju kahjustamiseks läbiksid vaktsiinid vere-aju barjääri; siiski tuleb seda pidada võimalikuks, eriti pärast korduvat süstimist, ning see võib raskendada entsefaliidi kliinilist kulgu.
1. Millised tõendid on praegu kättesaadavad, näitamaks, et mRNA vaktsiiniosakesed tungivad läbi vere-aju barjääri?
Seda küsimust ei ole konkreetselt inimestel ega loomadel uuritud. Järgnevalt antakse ülevaade olemasolevatest piiratud tõenditest.
1.1. Loomkatsed mudelvaktsiinidega
Nii Pfizer [1] kui ka Moderna [2] on läbi viinud loomkatseid mudelvaktsiinidega, mis sisaldavad samu lipiide kui vastavad COVID-19 vaktsiinid, kuid erinevat mRNA-d. Mõlemal juhul leiti nende mudelvaktsiinide komponente ka ajukoest; Pfizer tuvastas lipiidikomponendi ja Moderna tuvastas mRNA. Mõlemal juhul olid kontsentratsioonid ajukoes oluliselt madalamad kui veres. Kuid nagu allpool selgub, ei tähenda need leiud, et need vaktsiinid aju ei kahjustaks.
1.2. Vere-aju barjääri kaudu transportimise mehhanismist
In vivo omandavad Pfizeri ja Moderna vaktsiinides kasutatavad lipiidide nanoosakesed “biomolekulaarse koroona” ehk keha enda valkudest koosneva väliskatte. Selle kattega käituvad nad seejärel sarnaselt keha enda looduslike rasva transpordiosakestega, lipoproteiinidega. Lipiidide nanoosakeste rakulist omastamist ja nende transportimist läbi vere-aju barjääri vahendatakse eelkõige valkudega ApoB ja ApoE [3,4], mis täidavad sama eesmärki ka keha enda lipoproteiinidega.
1.3. Kas ogavalk võib mõjutada transporti läbi vere-aju barjääri?
Kuigi lipiidide nanoosakesed on olulised, ei tohiks tähelepanuta jätta vaktsiinis sisalduva mRNA võimalikku rolli. On teada, et SARS-CoV-2 ogavalk võib kahjustada vere-aju barjääri funktsiooni [5–8]. Üsna võimalik, et vaktsiiniosakesi võivad esialgu omastada ajuvälised rakud, mis seejärel toodavad ja vabastavad ogavalku vereringesse. See ringlev ogavalk võib seejärel mõjutada vere-aju barjääri ja hõlbustada edasiste vaktsiiniosakeste läbipääsu ajukoesse. Seega oleks olnud väga oluline teha need loomkatsed tegelike COVID-19 vaktsiinidega, mitte ainult mudelvaktsiinidega. See ei oleks olnud tehnilisest seisukohast eriti keeruline. Suure tõenäosusega viisid tootjad need uuringud läbi, kuid otsustasid hoida tulemusi enda teada või jätsid nad need katsed tahtlikult vahele, et vältida neile ebasoodsate tulemuste saamise võimalust.
1.4. Vere-aju barjäär ja korduvad süstid
Vere-aju barjäär koosneb kahest rakukihist: väikeste veresoonte endoteel moodustab sisemise kihi ja ümbritseva ajukoe gliiarakud moodustavad välimise kihi. On hästi teada, et vere-aju barjäär muutub põletiku ajal läbilaskvaks. Kuni pole tõestatud vastupidist, tuleb eeldada, et see kehtib ka aju veresoonte põletiku (vaskuliit) kohta, mille põhjustasid mRNA vaktsiinid; see, et need vaktsiinid põhjustavad tõepoolest vaskuliidi erinevaid vorme, on nüüd uuringutes [9–14] piisavalt dokumenteeritud.
Selle taustal tundub tõenäoline, et mRNA vaktsiini esimene süst võib põhjustada aju veresoonte põletikku, mis pehmendab vere-aju barjääri. Teise süstiga sisestatavad vaktsiiniosakesed võivad seejärel takistamatult ajukoesse liikuda. Seetõttu ei piisa sellest, kui uurida mRNA vaktsiinide transportimist läbi vere-aju barjääri alles pärast ühte süsti, nagu tegid Pfizer ja Moderna oma loomkatsetes; selle asemel oleks pidanud transport olema mõõdetud ka pärast korduvaid süste.
1.5. Vaktsiinide juhuslik intravenoosne süstimine
COVID-19 vaktsiine süstitakse intramuskulaarselt (lihasesiseselt). Selle kasutusviisiga püütakse kõnealust ravimit või vaktsiini viia ekstratsellulaarsesse ruumi väljaspool vereringet, nii et see jääks vähemalt esialgu kudedesse; sealt võib see siis vereringesse jõuda ainult aeglaselt või üldse mitte. Eespool nimetatud tootjate loomkatsetest selgus, et tõepoolest suur osa lihasesiseselt süstitud mudelvaktsiinidest jäi lihaskoesse. Erinevate riiklike ja rahvusvaheliste reguleerivate ametite avaldatud riskihinnangutes eeldatakse, et see jääb alati nii.
Iga arst peaks siiski teadma, et isegi hoolika tehnika korral – st eelneva aspiratsiooniga [15–17] – võib süstimine toimuda kogemata vereringesse. Loomkatsetes on täheldatud, et mRNA vaktsiinide põhjustatud müokardiit on pärast intravenoosset manustamist raskema kuluga kui pärast intramuskulaarset süstimist [18]. Sama tuleb eeldada ka inimeste elundite, sealhulgas aju kahjustuste kohta.
1.6. Järeldus
Kokkuvõtteks võib öelda, et olemasolevatest andmetest ei piisa mRNA vaktsiinide transpordi usaldusväärseks kvantitatiivseks hindamiseks läbi vere-aju barjääri, kuid need siiski tõestavad kvalitatiivselt, et lipiidide nanoosakesed sisenevad ajju. Vaktsineerimist reguleerivate asutuste optimistlikes hinnangutes selles küsimuses ei võeta arvesse tõsiseid riske ja olulist segadust tekitavaid tegureid ning seetõttu on need ebarealistlikud.
2. Kui kaua võivad vaktsiini nanoosakesed ajju jääda?
Kõigepealt tuleks selgitada, et nanoosakesed kui sellised ei kesta tõenäoliselt kusagil kehas väga kaua – varsti pärast rakku imendumist eralduvad lipiidid RNA-st. Alles pärast seda, kui RNA on sel viisil vabastatud, võib see algatada ogavalgu sünteesi rakus. Sellest hetkest alates otsustab bioloogilise aktiivsuse ajavahemiku tõenäoliselt RNA stabiilsus, kuigi lipiidikomponendid võivad kaasa aidata ka mRNA vaktsiini toksilisusele.
Nagu ajju transportimise küsimuses, ei ole tootjad esitanud piisavaid ja usaldusväärseid andmeid vaktsiini mRNA-de püsivuse kohta ajukoes. EMA [Euroopa Ravimiamet] dokument Moderna kohta sisaldab jällegi andmeid ainult mudelvaktsiini, mitte tegeliku COVID-vaktsiini kohta. Väidetavalt jäi mudelvaktsiini mRNA kolm päeva pärast süstimist tuvastatavaks ainult lihaskoes, lümfisõlmedes ja põrnas. Pfizer ei teatanud RNA otsestest mõõtmistest, vaid ainult andmetest mudelvaktsiiniga kodeeritud valgu (lutsiferaasi) aktiivsuse kohta. See lagunes umbes ühepäevase poolestusajaga [1]. Loomade ajusid siiski ei analüüsitud.
Mõlemal juhul jääb ebaselgeks, mil määral kehtivad need loomkatsete tulemused SARS-CoV-2 ogavalku kodeeriva mRNA eluea kohta inimese ajus. Järgmises osas näeme, et on alust uskuda, et vaktsineerimisest põhjustatud ogavalgu ekspressioon inimese ajus võib kesta palju kauem, kui asjakohased loomkatsete andmed näitavad.
3. Millist kahju võivad vaktsiini nanoosakesed ajule põhjustada?
Peaksime kohe alguses märkima, et ajukahjustuste puhul on vere-aju barjäär vähem oluline, kui võiks eeldada; põhjused selguvad järgnevalt.
3.1. Insult
Nüüdseks on selge, et geneetiliselt muundatud COVID-vaktsiinide (nii mRNA- kui ka adenoviirusel põhinevate) põhjustatud kõrvaltoimed algavad väga sageli veresoonte kahjustusega (vt joonis 1). Vaskulaarne vigastus viib seejärel verehüüvete tekkeni; koed ja elundid, mille verevarustus sõltub nendest ummistunud veresoontest, saavad siis kahjustada või isegi hukkuvad. Insult ja südameatakk on selle patogeneetilise mehhanismi lihtsad ja praktiliselt olulised näited [19–21]. Teine võimalus on verejooks pärast vaktsiinist põhjustatud põletiku all kannatavate veresoonte rebenemist [22–24]. Selliste vigastuste vormide puhul piisab, kui vaktsiiniosakesed viiakse ringlevast verest veresoonte seinte rakkudesse. Need rakud ekspresseerivad seejärel ogavalku, võõrast antigeeni, ja tekitavad seeläbi immuunsüsteemi ärrituse, mis seejärel põhjustab tegelikku kahju. Pange tähele, et selle stsenaariumi korral ei pea osakesed ületama ühtegi peamist anatoomilist barjääri; ja eelkõige ei pea nad ületama vere-aju barjääri, et kahjustada aju veresooni ja põhjustada insulti.
Joonis 1: Kuidas COVID-19 mRNA vaktsiinid kahjustavad veresooni ja põhjustavad vere hüübimist. Pärast vaktsiini lipiidide nanoosakeste sisenemist ringlusse võtavad endoteelirakud need üle ja mRNA vabaneb. Seejärel ekspresseeritakse ogavalk; mõned molekulid on killustunud ja esitatud rakupinnal spetsiaalse kandjavalgu (MHC1) poolt. See põhjustab tsütotoksiliste T-rakkude rünnaku endoteelirakkudele. Hävitatud endoteelirakud lagunevad, hõlbustades vaktsiiniosakeste lekkimist külgnevatesse kudedesse. See avab verele ka veresoone seina sügavamad kihid, mis käivitab trombotsüütide agregatsiooni ja vere hüübimise.
3.2. Aju ja seljaaju põletik
Lisaks insuldile on mRNA vaktsiinid põhjustanud ka palju entsefaliidi ja müeliidi juhtumeid ehk vastavalt aju- ja seljaajupõletikku ning mõnikord ka mõlemat korraga (entsefalomüeliit). Patogeneetilised mehhanismid on kõigi kolme haiguse puhul samad; lihtsuse huvides kasutame järgnevalt ainult terminit “entsefaliit”.
3.2.1. Entsefaliit ogavalgu vastase immuunreaktsiooni tõttu
Tuleb eeldada, et see patogeneetiline mehhanism toimib immunoloogia esimestest põhimõtetest lähtuvalt. Kuidas saaks seda tõestada entsefaliidi korral? Järgmised kriteeriumid muudaksid sellise diagnoosi vähemalt väga tõenäoliseks:
Tuleb märkida, et 2. ja 3. kriteeriumi saab täita ainult histopatoloogiliste uuringutega; ajuga tehakse need tavaliselt alles pärast lahkamist, kuna selle organi biopsia on eriti ebakindel.
Kuigi see mehhanism on tõenäoliselt väga oluline, on toetavaid tõendeid seni vähe – lihtsalt seetõttu, et patoloogid pole seda otsinud. Siiski avaldati äsja esimene juhtumiaruanne, mis vastab kõigile eespool nimetatud kriteeriumidele [25] (vt joonis 2). See väga hoolikas uuring välistas ka selle, et ogavalgu tuvastatud ekspressiooni põhjustas viirusega nakatumine, mitte vaktsineerimine.
Kõnealune patsient oli esialgu saanud ühe AstraZeneca [COVID-19] adenoviirusel põhineva süsti, millele järgnes kaks Pfizeri [COVID-19] mRNA süsti. Viimane süst oli tehtud kolm nädalat enne patsiendi surma. Ogavalgu märgatav ekspressioon tuvastati aju kapillaarides ja ka ajukoe gliiarakkudes, mis oli väga tõenäoliselt põhjustatud viimasest mRNA vaktsiini annusest. Seetõttu tuleb eeldada, et ogavalk säilib pärast mRNA vaktsiinide manustamist vähemalt mitu nädalat ja tõenäoliselt sünteesitakse seda selle aja jooksul pidevalt. See leid kordab varasemaid uuringuid erinevate kudede kohta peale aju ja vere [26–29]. Ogavalgu ekspressioon gliiarakkudes näitab ka ühemõtteliselt, et üks või mõlemad vaktsiinid võivad läbida vere-aju barjääri.
Pilt 2: SARS-CoV-2 ogavalgu tuvastamine ajukoes vaktsiini poolt indutseeritud entsefaliidiga surnud patsiendilt immunohistokeemia abil. Pruuni pigmendi ladestumine näitab ogavalgu olemasolu väikese veresoone seinas (punane nool) ja ümbritseva ajukoe mitmes gliiarakus (sinine nool). Foto: Michael Mörz [25].
3.2.2. Autoimmuunne entsefaliit
Selles patogeneetilises mehhanismis on seos vaktsineerimisega kaudne: vaktsiin vallandab kõigepealt põletiku, mis ei pruugi isegi aju otseselt mõjutada; ja selle põletiku kontekstis aktiveeritakse immuunvastus mitte ainult ogavalgu, vaid ka ühe või mitme keha enda valgu või muude biomolekulide (autoantigeenide) vastu. Immuunsüsteem võib seejärel rünnata neid samu autoantigeene algselt mõjutamata sihtorganites, sealhulgas ajus, ja vallandada ka seal põletiku.
Kliinilised sümptomid ja ka lahkamisleiud rutiinsete meetodite kasutamisel on tõenäoliselt väga sarnased nagu immuunreaktsiooni korral ogavalgule. Seega, kuidas saaks otsustada, kas entsefaliiti vallandab ogavalk või autoantigeen? Tõelise autoimmuunse entsefaliidi korral tuleb oodata järgmisi leide:
Jarius jt [30] teatasid autoantikeha-positiivse entsefaliidi juhtumist patsiendil, kes oli algselt saanud kaks annust AstraZeneca adenoviirusel põhinevat vaktsiini, millele järgnes üks annus Pfizeri mRNA vaktsiini. Sellel patsiendil oli ajus ekspresseeritud valk – müeliin oligodendrotsüütide glükoproteiin (MOG) – autoantigeen. Need autorid andsid ülevaate ka kahekümnest muust kirjanduses varem kajastatud juhtumist. Neist kolmel juhul oli kasutatud mRNA vaktsiini, ülejäänud seitseteist juhtumit olid seotud AstraZeneca vaktsiiniga. Kuna ükski neist juhtudest ei olnud surmav, ei saadud positiivseid ega negatiivseid histopatoloogilisi tõendeid ogavalgu ekspressiooni kohta.
Asioli jt [31] teatasid neljast entsefaliidi juhtumist, kus avastati LGI1 valgu vastased autoantikehad. Kolm neist juhtudest, kõik samast linnast (Bologna), toimusid pärast mRNA vaktsiinide süstimist. Eriti silmatorkavast juhtumist teatasid Poli jt. [32]. Sellel patsiendil tekkis samaaegselt kolm erinevat autoimmuunhaigust – demüeliniseeriv entsefaliit, müasteenia ja türeoidiit. Siiski ei tuvastatud spetsiifilisi autoantikehasid, mis võiksid antud juhul entsefaliiti põhjustada.
3.2.3. Antikehanegatiivne autoimmuunne entsefaliit
Mitmel juhul teatati entsefaliidist pärast mRNA vaktsiinide süstimist, diagnoositi “antikehanegatiivne autoimmuunne entsefaliit” [33–35]. Kindlasti on mõistlik eeldada, et paljudel sellistel juhtudel võis tuvastamata autoantigeen olla põhjuslik. Teisest küljest on ilma histopatoloogiata sageli võimatu otsustada, kas antud entsefaliidi juhtum oli põhjustatud immuunreaktsioonist tundmatu autoantigeeni või ogavalgu vastu.
3.3. Järeldus
Pärast mRNA vaktsiinide ja ka adenoviirusel põhinevate vaktsiinide kasutamist on teatatud paljudest entsefaliidi, müeliidi ja entsefalomüeliidi juhtudest. Nii autoimmuunreaktsioonid kui ka immuunreaktsioon ogavalgu vastu on tõestatud konkreetsetel juhtudel põhjuslikuks. Iga vormi vastavat osakaalu kõigi entsefaliidi kliiniliste juhtude koguarvus ei saa praegu kättesaadavate tõendite põhjal kindlaks määrata.
4. Kokkuvõte
Pärast mRNA vaktsiinide kasutamist COVID-19 vastu on arvukalt teateid kesknärvisüsteemi häiretest. Nende häirete hulka kuuluvad insult, ajuverejooks ja entsefaliit. Ei ole vajalik, et aju kahjustamiseks läbiksid vaktsiinid vere-aju barjääri; siiski tuleb seda pidada võimalikuks, eriti pärast korduvat süstimist või juhuslikku intravenoosset süstimist, ning see võib raskendada entsefaliidi kliinilist kulgu.
Viited:
PDF-fail on allalaadimiseks saadaval: COVID-19 vastased mRNA vaktsiinid ja nende mõju kesknärvisüsteemile
Toimetas Sander Soomaa
Kommentaarid
Kommentaare lugeda ja kommenteerida saavad vaid Minu Telegrami tellinud kasutajad. Tellimuse esitamiseks kliki siia või logi sisse siit.